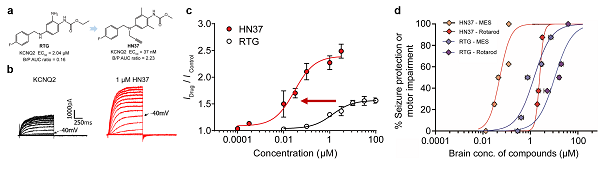
癲癇是神經(jīng)內(nèi)科重大疾病之一����,發(fā)病率接近1%�,中國(guó)有近1000萬(wàn)癲癇患者�����。其中�,約三分之一的癲癇患者對(duì)現(xiàn)有藥物均不敏感,被稱(chēng)為難治性癲癇���。KCNQ鉀通道包括KCNQ1 ~ KCNQ5五個(gè)亞型�����,其中KCNQ2是確證的癲癇治療靶點(diǎn)�����。首個(gè)靶向KCNQ2通道的抗癲癇藥物瑞替加濱(Retigabine��,RTG)于2011年上市�,但存在嚴(yán)重的劑量相關(guān)的皮膚及視網(wǎng)膜色素沉積等毒副作用,其原研公司葛蘭素史克(GSK)基于商業(yè)原因于2017年將其主動(dòng)撤市�����。高效但沒(méi)有色素沉積等副作用是靶向KCNQ2抗癲癇藥物研發(fā)的一個(gè)方向�,特別隨著抗抑郁等擴(kuò)展適應(yīng)癥研究結(jié)果披露,KCNQ2近年來(lái)備受關(guān)注�����。派恩加濱(Pynegabine�����,HN37)由中國(guó)科學(xué)院上海藥物研究所自主研發(fā)����,已推進(jìn)至臨床II期研究階段,國(guó)內(nèi)權(quán)益已轉(zhuǎn)讓�����。與瑞替加濱相比,派恩加濱的化學(xué)性質(zhì)��、活性���、藥代和安全性特征均顯著優(yōu)化���,沒(méi)有色素沉積風(fēng)險(xiǎn),在包括難治性癲癇在內(nèi)的多種動(dòng)物模型上顯示良好抗癲癇效應(yīng)(圖1)����。臨床I期試驗(yàn)證明其具有良好的安全和代謝特性。派恩加濱作為新一代靶向KCNQ通道的抗癲癇藥物�����,有望為眾多難治性癲癇患者提供藥物治療新選擇�。
上海藥物所高召兵課題組圍繞與神經(jīng)系統(tǒng)重大疾病有關(guān)的離子通道為中心���,致力于推進(jìn)離子通道新機(jī)制���、新功能研究,發(fā)現(xiàn)新型離子通道���,研發(fā)離子通道新藥����。課題組在KCNQ通道相關(guān)的抗癲癇/鎮(zhèn)痛藥物發(fā)現(xiàn)和機(jī)制研究中與合作者共同開(kāi)展了系列研究工作:建立高通量篩選體系發(fā)現(xiàn)一系列KCNQ小分子激動(dòng)劑( Mol Pharm. 2015; Acta Pharmacol Sin. 2016; JMC. 2020);證明激活外周KCNQ通道可有效鎮(zhèn)痛( Pain. 2015);揭示了KCNQ2通道小分子激動(dòng)劑的亞型選擇性直接受胞內(nèi)信號(hào)通路調(diào)節(jié)����,與細(xì)胞膜二磷酸磷脂酰肌醇(PIP2)水平直接相關(guān)( PNAS. 2013a);結(jié)合分子模擬模擬�����,揭示了PIP2增強(qiáng)KCNQ2電壓敏感性動(dòng)態(tài)調(diào)節(jié)機(jī)制��,發(fā)現(xiàn)了新的PIP2 結(jié)合位點(diǎn)( PNAS. 2013b)��;證明一個(gè)通道結(jié)合一個(gè)小分子激動(dòng)劑即可實(shí)現(xiàn)藥理學(xué)效應(yīng)( Cell Res. 2016); 證明抗癲癇新藥派恩加濱在自發(fā)性癲癇發(fā)作的點(diǎn)突變小鼠模型上具有較好的治療效應(yīng)��,提示KCNQ2通道激動(dòng)劑類(lèi)藥物可能對(duì)KCNQ2突變致先天性癲癇有治療效果( Neurobiol Dis. 2022)�����;采用CRISPR/Cas9技術(shù)修復(fù)KCNQ2通道單點(diǎn)突變�,率先在動(dòng)物體內(nèi)水平實(shí)現(xiàn)遺傳性癲癇的基因治療( Acta Pharmacol Sin. 2023)。
派恩加濱作為新一代KCNQ2通道激動(dòng)劑��,理解其強(qiáng)效激動(dòng)KCNQ2通道的分子作用機(jī)制對(duì)指導(dǎo)臨床實(shí)驗(yàn)和KCNQ通道藥物研發(fā)均有重要意義。為此�����,課題組聯(lián)合浙江大學(xué)郭江濤教授開(kāi)展合作研究���。2023年10月19日�����,聯(lián)合團(tuán)隊(duì)在 Nature Communications 發(fā)表研究論文“Ligand activation mechanisms of human KCNQ2 channel”�,報(bào)道了人源KCNQ2- HN37和PIP2復(fù)合物的結(jié)構(gòu)��,揭示了派恩加濱的分子作用機(jī)制����。冷凍電鏡結(jié)構(gòu)顯示1個(gè)KCNQ2亞基可結(jié)合2個(gè)HN37分子,表明1個(gè)KCNQ2通道最多可結(jié)合8個(gè)HN37分子�����;通過(guò)比較關(guān)閉態(tài)和開(kāi)放態(tài)的KCNQ2的結(jié)構(gòu)���,并結(jié)合其它KCNQ2激動(dòng)劑大麻二酚(CBD)等的結(jié)合模式��,該論文對(duì)KCNQ2激動(dòng)劑作用機(jī)制進(jìn)行了較為全面的分析�。
不同于對(duì) KCNQ2增強(qiáng)活性較弱的小分子激動(dòng)劑RTG(KCNQ2-CaMRTG)��,1個(gè)KCNQ2亞基中僅結(jié)合1個(gè)RTG小分子��;在KCNQ2-CaMHN37結(jié)構(gòu)中����,1個(gè)KCNQ2亞基結(jié)合2個(gè)HN37分子:HN37A和HN37B(圖2a和b)。其中����,HN37A結(jié)合于RTG結(jié)合口袋(圖2c),表明它可能與RTG的激活機(jī)制相同����;而HN37B結(jié)合在電壓感受區(qū)(VSD)和孔道區(qū)(PD)的界面處(圖2d)。結(jié)合口袋獲電生理研究證實(shí)��。結(jié)合更多結(jié)構(gòu)和電生理研究�����,論文推測(cè)HN37B可能有穩(wěn)定HN37A的作用��,或可部分發(fā)揮PIP2的功能。派恩加濱不同于瑞替加濱的兩組結(jié)合位點(diǎn)�,以及本研究揭示的與PIP2潛在的相互作用,可能是其強(qiáng)效激動(dòng)活性的分子基礎(chǔ)����。
浙江大學(xué)基礎(chǔ)醫(yī)學(xué)院博士生馬德敏和李瀟瀟、上海藥物所鄭月明副研究員和周曉宇博士為論文的共同第一作者����。浙江大學(xué)基礎(chǔ)醫(yī)學(xué)院郭江濤教授和上海藥物所高召兵研究員為共同通訊作者。該工作還得到派恩加濱共同發(fā)明人上海藥物所南發(fā)俊研究員, 浙江大學(xué)醫(yī)學(xué)院楊巍教授���、蘇楠楠教授��、趙國(guó)華教授�、方嘉佳教授和澳門(mén)科技大學(xué)侯盼盼助理教授的大力支持��;電鏡數(shù)據(jù)收集工作得到浙江大學(xué)冷凍電鏡中心的大力支持����。本研究受?chē)?guó)家自然科學(xué)基金、浙江省自然科學(xué)基金�、國(guó)家杰出青年科學(xué)基金�����、國(guó)家科技創(chuàng)新2030重大計(jì)劃和中國(guó)科學(xué)院青年創(chuàng)新促進(jìn)會(huì)、國(guó)家重點(diǎn)研發(fā)計(jì)劃等項(xiàng)目的資助��。
圖1. 抗癲癇候選新藥派恩加濱(Pynegabine�,HN37)
圖2. 結(jié)合HN37的KCNQ2-CaM結(jié)構(gòu)(KCNQ2-CaMHN37)
(供稿部門(mén):高召兵課題組)