腫瘤微環(huán)境(TME)是指由腫瘤細(xì)胞�����、免疫細(xì)胞等多種細(xì)胞與各種信號(hào)分子所構(gòu)成的復(fù)雜生態(tài)系統(tǒng)�����,并隨著腫瘤進(jìn)程發(fā)生變化����。免疫檢查點(diǎn)抑制劑如PD-1/PD-L1抗體通過恢復(fù)腫瘤殺傷性CD8 +T細(xì)胞功能,提高腫瘤微環(huán)境中CD8 +T細(xì)胞數(shù)量與活性��,從而提高機(jī)體免疫監(jiān)察能力發(fā)揮抗腫瘤效應(yīng)����。盡管這種治療方式使得部分病人能夠獲得長(zhǎng)期生存受益,在腫瘤治療領(lǐng)域取得了重大成功��,但是腫瘤病人腫瘤微環(huán)境復(fù)雜多變的特性常常導(dǎo)致腫瘤浸潤(rùn)的CD8 +T細(xì)胞數(shù)量不足或喪失活性���,從而使超過70%的腫瘤病人無法有效響應(yīng)免疫檢查點(diǎn)療法即對(duì)免疫檢查點(diǎn)抑制劑產(chǎn)生了先天性耐藥或者獲得性耐藥��。由于免疫檢查點(diǎn)療法的耐藥性問題極大地限制了該療法的臨床應(yīng)用�����,所以�����,如何克服免疫檢查點(diǎn)抑制劑耐藥性問題成為腫瘤免疫研究的熱點(diǎn)問題����。
為了發(fā)現(xiàn)能夠調(diào)節(jié)腫瘤微環(huán)境中CD8 +T抗腫瘤免疫的新靶點(diǎn),為克服免疫檢查點(diǎn)抑制劑耐藥性提供新的策略與思路�,中國(guó)科學(xué)院上海藥物研究所羅成課題組聯(lián)合哈爾濱工業(yè)大學(xué)劉川鵬課題組,發(fā)展了基于轉(zhuǎn)錄組數(shù)據(jù)預(yù)測(cè)腫瘤免疫調(diào)控靶標(biāo)的計(jì)算生物學(xué)方法���,并發(fā)現(xiàn)精氨酸甲基轉(zhuǎn)移酶1(PRMT1)是調(diào)控黑色素腫瘤微環(huán)境中CD8 +T細(xì)胞浸潤(rùn)與活化的新靶標(biāo)�����,且實(shí)驗(yàn)室自主研發(fā)的PRMT1小分子抑制劑能夠顯著提高腫瘤微環(huán)境中CD8 +T細(xì)胞的數(shù)量與活性���,抑制腫瘤生長(zhǎng)并提高耐藥黑色素瘤對(duì)PD-1抗體治療的敏感性。該研究論文于2023年11月22日在線發(fā)表于 Cancer Research��。

前期研究中���,羅成課題組圍繞表觀遺傳調(diào)控蛋白先導(dǎo)化合物發(fā)現(xiàn)和化學(xué)干預(yù)研究開展系統(tǒng)研究�����,針對(duì)蛋白精氨酸甲基轉(zhuǎn)移酶家族PRMT1�、PRMT4��、PRMT5����、PRMT6蛋白獲得了一系列高活性、高選擇性�、母核結(jié)構(gòu)全新的小分子抑制劑(J Med Chem. 2012;55:7978;J Med Chem. 2017;60:8888.;J Med Chem. 2017;60:6289)�,并以自主研發(fā)的PRMT1、PRMT5小分子為化學(xué)探針揭示了PRMT家族在腫瘤干性調(diào)控�����、腫瘤耐藥調(diào)控方面的全新功能��,為PRMT1���、PRMT5抑制劑的臨床適應(yīng)癥應(yīng)用拓展提供了重要科學(xué)依據(jù)���。此外,團(tuán)隊(duì)與海軍軍醫(yī)大學(xué)附屬長(zhǎng)征醫(yī)院謝渭芬主任合作��,發(fā)現(xiàn)PRMT5抑制劑通過下調(diào)肝細(xì)胞核因子HNF4 轉(zhuǎn)錄降低肝癌干性相關(guān)基因表達(dá)����,具有抗肝癌生長(zhǎng)活性(Theranostics. 2019,13;9(9):2606-2617)。與上海交通大學(xué)醫(yī)學(xué)院附屬仁濟(jì)醫(yī)院張進(jìn)主任合作發(fā)現(xiàn)PRMT1抑制劑可克服腎透明細(xì)胞癌一線藥物舒尼替尼耐藥�,揭示PRMT1調(diào)控耐藥逃逸通路LCN2-pAKT-pRb激活��、導(dǎo)致舒尼替尼耐藥的表觀遺傳機(jī)制��,并提出PRMT1抑制劑克服腎癌耐藥的聯(lián)用治療新策略(Theranostics. 2021,11(11):5387-5403)���。與中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心高棟研究員合作,發(fā)現(xiàn)代謝物精胺抑制去勢(shì)抵抗性前列腺腫瘤生長(zhǎng)并克服恩雜魯胺耐藥的新功能���,揭示代謝物作用于表觀遺傳靶標(biāo)PRMT1調(diào)控腫瘤耐藥的表觀遺傳分子機(jī)制����,并提出PRMT1抑制劑可作為去勢(shì)抵抗性前列腺腫瘤治療的新策略(Cell Rep. 2023,42(7):112798)�����。近年來�����,課題組通過開展腫瘤免疫調(diào)控新靶標(biāo)和小分子研究���,發(fā)現(xiàn)了代謝物L(fēng)-5-羥基色氨酸抑制PD-L1/L2表達(dá)而激活T細(xì)胞抗腫瘤免疫的新功能�����,為L(zhǎng)-5-HTP應(yīng)用于癌癥免疫治療以及改善腫瘤患者的抑郁行為提供了理論依據(jù)(J Immunother Cancer. 2022,10(6):e003957)�,發(fā)現(xiàn)了可調(diào)控髓系抑制細(xì)胞MDSC提高放療和放療免疫檢查點(diǎn)聯(lián)合治療效果的“m6A閱讀子”YTHDF2小分子抑制劑(Cancer Cell. 2023,41(7):1294-1308)�。
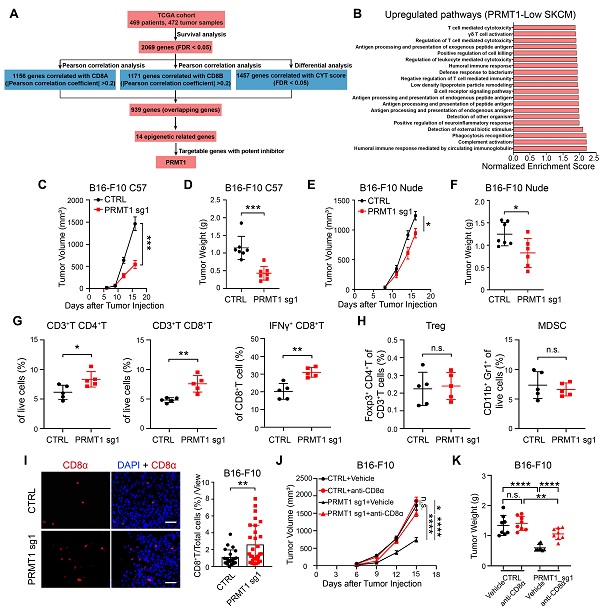
在前期研究基礎(chǔ)上,團(tuán)隊(duì)綜合表達(dá)了差異��、生存分析����、CD8 +T細(xì)胞相關(guān)性分析、免疫活細(xì)胞殺傷性評(píng)分(CYT)等序貫篩選�,發(fā)展了腫瘤殺傷性T細(xì)胞調(diào)控靶標(biāo)預(yù)測(cè)的計(jì)算生物學(xué)方法,并基于TCGA數(shù)據(jù)庫469位黑色素瘤患者基因表達(dá)譜進(jìn)行分析和篩選���,發(fā)現(xiàn)了抑制黑色素腫瘤微環(huán)境內(nèi)CD8 +T細(xì)胞浸潤(rùn)與激活的潛在新靶標(biāo)PRMT1�。團(tuán)隊(duì)經(jīng)過進(jìn)一步動(dòng)物水平功能評(píng)價(jià)��,確證了PRMT1敲除顯著降低同系免疫完整小鼠上黑色素腫瘤內(nèi)的CD8 +T細(xì)胞數(shù)量和IFN +CD8 +T比例���,延緩腫瘤生長(zhǎng)����,而在免疫缺陷荷瘤小鼠上PRMT1敲除對(duì)腫瘤生長(zhǎng)的抑制作用顯著降低�����。同系免疫完整小鼠模型上,CD8 +T細(xì)胞中和抗體顯著降低了PRMT1敲除的腫瘤生長(zhǎng)抑制作用�。表明敲除黑色素細(xì)胞內(nèi)源PRMT1能夠增加腫瘤組織內(nèi)CD8 +T細(xì)胞與活性,并以CD8 +T細(xì)胞依賴的方式發(fā)揮顯著的抗腫瘤效應(yīng)��。
圖1. PRMT1抑制黑色素瘤微環(huán)境中T細(xì)胞的浸潤(rùn)與激活
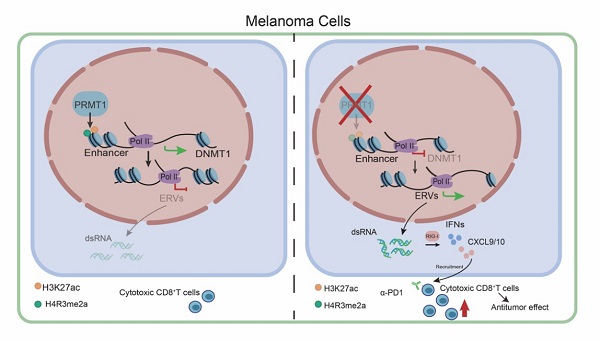
結(jié)合轉(zhuǎn)錄組與染色質(zhì)免疫共沉淀組分析�,機(jī)制研究發(fā)現(xiàn)敲除黑色素細(xì)胞內(nèi)PRMT1能夠降低DNA甲基轉(zhuǎn)移酶1(DNMT1)基因的增強(qiáng)子區(qū)域H4R3me2a與H3K27ac修飾水平,抑制增強(qiáng)子活性��,降低DNMT1的轉(zhuǎn)錄表達(dá)����。下調(diào)的DNMT1進(jìn)一步激活了腫瘤細(xì)胞內(nèi)逆轉(zhuǎn)錄病毒元件(ERVs)的轉(zhuǎn)錄表達(dá),并促進(jìn)ERV來源的雙鏈RNA(dsRNA)在細(xì)胞質(zhì)內(nèi)累積���,進(jìn)而激活dsRNA識(shí)別通路與I型干擾素通路����,最終促進(jìn)I型干擾素下游的T H1型趨化因子CXCL9/10/11的表達(dá)����。T H1型趨化因子被報(bào)道能夠有效的招募CD8 +T細(xì)胞至腫瘤組織內(nèi)部并促進(jìn)CD8 +T細(xì)胞的激活。至此,該研究闡明了PRMT1調(diào)控黑色素腫瘤微環(huán)境內(nèi)CD8 +T細(xì)胞浸潤(rùn)與激活的表觀遺傳分子機(jī)制����。
圖2 PRMT1調(diào)控DNMT1-ERVs-dsRNA-IFNs信號(hào)通路模式圖
最終,運(yùn)用自主開發(fā)的PRMT1的抑制劑DCPT1061����,研究團(tuán)隊(duì)評(píng)估了PRMT1抑制劑聯(lián)合免疫檢查點(diǎn)抑制劑PD-1抗體在低免疫原性����、PD-1抗體治療不響應(yīng)的黑色素腫瘤模型中的抗腫瘤效應(yīng)。結(jié)果表明��,在對(duì)免疫檢查點(diǎn)抑制劑治療原發(fā)性耐藥的B16-F10黑色素腫瘤上���,PRMT1抑制劑DCPT1061增加腫瘤浸潤(rùn)C(jī)D8 +T細(xì)胞的數(shù)量與活性�,提高耐藥黑色素瘤對(duì)PD-1抗體治療的敏感性���。
綜上所述��,該研究開發(fā)了腫瘤殺傷性T細(xì)胞調(diào)控靶標(biāo)預(yù)測(cè)的計(jì)算生物學(xué)方法����,發(fā)現(xiàn)了PRMT1是黑色素腫瘤微環(huán)境CD8 +T細(xì)胞浸潤(rùn)和活性調(diào)控的重要靶標(biāo),闡明了表觀修飾酶PRMT1參與CD8 +T細(xì)胞相關(guān)腫瘤免疫調(diào)節(jié)的全新功能與表觀遺傳分子機(jī)制��,提示了PRMT1抑制劑在腫瘤免疫治療���、克服免疫檢查點(diǎn)抑制劑耐藥方面的應(yīng)用前景���。
上海藥物所與哈爾濱工業(yè)大學(xué)聯(lián)合培養(yǎng)博士研究生陶泓儒、南京中醫(yī)藥大學(xué)碩士研究生金晨�、中國(guó)科學(xué)院杭州高等研究院碩士研究生周禮源及上海交通大學(xué)附屬新華醫(yī)院主治醫(yī)師鄧振忠為該論文的共同第一作者。上海藥物所羅成研究員���、張?jiān)芯繂T和哈爾濱工業(yè)大學(xué)的劉川鵬副教授為該論文的共同通訊作者���。該研究還得到了中國(guó)科學(xué)院廣州生物醫(yī)藥與健康研究院孔祥謙研究員、德國(guó)海德堡大學(xué)盧俊彥教授����、浙江理工大學(xué)葉飛教授的支持,得到國(guó)家重點(diǎn)研發(fā)計(jì)劃�����、國(guó)家自然科學(xué)基金�����、上海市自然科學(xué)基金等項(xiàng)目的資助。